Đề khảo sát chất lượng học kỳ I môn Hóa học Lớp 8 - Mã đề 02 - Năm học 2011-2012 - Trường THCS Phù Hóa (Có đáp án)
Câu 3: (3.0đ)
Cho 5,6 gam Fe phản ứng hết với HCl thu được 12,7 gam FeCl2 và 2,24 lít H2 (đktc).
Áp dụng định luật bảo toàn khối lượng tính khối lượng HCl đã phản ứng?
Câu 4: (3.0đ)
Tính thành phần phần trăm ( theo khối lượng) của các nguyên tố trong hợp chất CuSO4 ?
Bạn đang xem tài liệu "Đề khảo sát chất lượng học kỳ I môn Hóa học Lớp 8 - Mã đề 02 - Năm học 2011-2012 - Trường THCS Phù Hóa (Có đáp án)", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
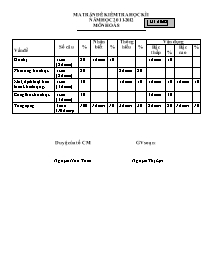
MA TRẬN ĐỀ KIỂM TRA HỌC KÌ I M· ®Ò:02 NĂM HỌC 2011-2012 MÔN HOÁ 8 Vấn đề Số câu % Nhận biết % Thông hiểu % Vận dụng Bậc thấp % Bậc cao % Hoá trị 1 câu (2 điểm) 20 1điểm 10 1điểm 10 Phản ứng hoá học 1 câu (2 điểm) 20 2 điểm 20 Mol, định luật bảo toàn khối lượng. 1 câu (3 điểm) 30 1 điểm 10 1điểm 10 1điểm 10 Công thức hoá học 1 câu (3 điểm) 30 3điểm 30 Tổng cộng 4 câu (10 điểm) 100 1 điểm 10 3 điểm 30 5 điểm 50 1 điểm 10 Duyệt của tổ CM GV soạn: Nguyễn Hữu Tuấn Nguyễn Thị Lợi TRƯỜNG THCS PHÙ HÓA ĐỀ KSCL HỌC KÌ I NĂM HỌC 2011- 2012 Mã đề:02 Số báo danh: Môn : Hoá học - Lớp 8 Thời gian làm bài 45 phút( không kể thời gian giao đề) ĐỀ RA: Câu 1: (2.0đ) a. Viết biểu thức quy tắc hóa trị? b. Tính hóa trị của Al trong Al2O3 (Biết hóa trị của O là II) Câu 2: (2.0đ) t0 Hoàn thành các phương trình phản ứng sau và cho biết tỷ lệ các chất trong phương trình? a. Al + O2 Al2O3 b. FeO + HCl FeCl2 + H2O Câu 3: (3.0đ) Cho 5,6 gam Fe phản ứng hết với HCl thu được 12,7 gam FeCl2 và 2,24 lít H2 (đktc). Áp dụng định luật bảo toàn khối lượng tính khối lượng HCl đã phản ứng? Câu 4: (3.0đ) Tính thành phần phần trăm ( theo khối lượng) của các nguyên tố trong hợp chất CuSO4 ? ( Biết NTK của Cu = 64 ; S = 32 ; O = 16 ) ****************************** Duyệt của tổ CM GV soạn: Nguyễn Hữu Tuấn Nguyễn Thị Lợi TRƯỜNG THCS PHÙ HÓA HƯỚNG DẪN CHẤM M· ®Ò:02 KSCL HỌC KÌ II NĂM HỌC 2011- 2012 M«n : HOÁ HỌC - Lớp 8 Câu 1: (2.0đ) a b Biểu thức quy tắc hóa trị: Trong hợp chất AxBy ta luôn có: a . x = b . y 0,5đ Với a, b là hóa trị của A ,B 0,25đ x , y là chỉ số ( số nguyên tử) của A , B. 0,25đ b. Hóa trị của Al trong Al2O3 (Biết hóa trị của O là II) Gọi a là hóa trị của Al 0,25đ Áp dụng biểu thức quy tắc hóa trị ta có: a . 2 = II . 3 0,25đ => a = III 0,25đ Vậy hóa trị của Al là III. 0,25đ Câu 2: (2.0đ) t0 Hoàn thành các phương trình phản ứng và cho biết tỷ lệ các chất trong phương trình: a. 4Al + 3O2 2Al2O3 0,5đ Tỷ lệ Al : O2 : Al2O3 = 4 : 3 : 2 0,5đ b. FeO + 2HCl FeCl2 + H2O 0,5đ Tỷ lệ FeO : HCl : FeCl2 : H2O = 1 : 2 : 1 : 1 0,5đ Câu 3: (3.0đ) Số mol khí H2 = 2,24 / 22,4 = 0,1 mol 0,5đ Khối lượng khí H2 thu được là : m = 2 . 0,1 = 0,2 gam 0,5đ Áp dụng định luật bảo toàn khối lượng ta có: 2 2 mFe + mHCl = mFeCl + mH 0,5đ 2 2 => mHCl = (mFeCl + mH ) - mFe 0,5đ mHCl = (12,7 + 0,2 ) - 5,6 = 7,3 gam 0,5đ Vậy khối lượng HCl phản ứng là 7,3 gam. 0,5đ Câu 4: (3.0đ) Khối lượng mol của CuSO4 là: 64 + 32 + 16 . 4 = 160 gam 0,5đ Thành phần % các nguyên tố: 4 Áp dụng công thức tính %Cu = (MCu . x) : MCuSO . 100% thay số vào ta có: 0,5đ %Cu = (64 . 1 ) : 160 . 100% = 40 % 0,5đ Tương tự ta có: % S = (32 . 1) : 160 . 100% = 20% 0,5đ % O = (16 . 4 ) : 160 . 100% = 40% 0,5đ Vậy trong CuSO4 có 40% Cu ; 20% S và 40% O. 0,5đ ********************************** Duyệt của tổ CM GV soạn:
Tài liệu đính kèm:
 de_khao_sat_chat_luong_hoc_ky_i_mon_hoa_hoc_lop_8_ma_de_02_n.doc
de_khao_sat_chat_luong_hoc_ky_i_mon_hoa_hoc_lop_8_ma_de_02_n.doc





